
우리 학교 생명과학과 김학성 교수와 서문형 박사 연구팀은 단백질이 생체 내 분자를 인식하고 기능을 수행하는데 중요한 단백질의 생체분자에 대한 결합력을 조절하는 메커니즘을 새롭게 밝혀냈다 .
연구 결과는 과학 분야의 권위지인 ‘ 네이처 커뮤니케이션즈 (Nature Communications)’ 24일자 온라인판에 게재됐다.
연구팀은 지난해에 단백질의 생체분자 인식 메커니즘을 최초로 밝혀내 Nature Chemical Biology 에 발표한데 이어 , 이번 연구를 통해 단백질이 생체분자에 대한 결합력을 조절하는 핵심 원리를 규명함으로써 생체 내 단백질의 기능과 조절 기작을 보다 명확하게 이해하는 데 크게 기여할 것으로 전망된다 .
효소나 항체 , 호르몬 등으로 대표되는 단백질은 모든 생명체 내에서 다양한 생체 분자를 특이적으로 인식하여 신호전달 , 면역반응 등을 정교하게 진행시켜 생명현상을 유지하고 조절하는데 가장 중요한 역할을 담당한다 . 이런 과정에서 단백질이 생체분자에 대한 결합력은 두 분자 사이의 결합지속 시간이 정해지고 , 단백질의 생체 내 기능을 결정하고 조절하는 핵심 요인이다 . 이번 연구 결과를 바탕으로 단백질 활성을 보다 정교하게 조절하는 것이 가능해질 것으로 예상된다 .
연구팀은 단백질들이 생체분자를 인식하는 과정에서 , 단백질의 생체분자에 대한 결합력은 두 분자 사이의 비 공유 상호작용의 크기뿐만 아니라 단백질의 고유한 동역학적 성질도 긴밀하게 연관되어 있다는 점에 주목했다 .
김 교수 연구팀은 단백질의 생체분자에 대한 결합력을 결정하는 기본 기작을 규명하기 위해 , 단백질의 allosteric site 에 돌연변이를 가하여 동일한 화학적 접촉면을 가지고 있지만 수십 배에서 수백 배의 결합력 차이를 보이는 다양한 돌연변이 단백질을 제작하였다 . 단백질의 allosteric site 는 생체분자와 직접 결합하는 부위는 아니지만 생체 분자 인식에 영향을 미치는 부위를 지칭한다 .
제작된 돌연변이 단백질들의 고유한 동역학적 성질을 단 분자 수준에서 실시간으로 분석하여 , 생체분자에 대한 결합력이 단백질의 고유한 동력학적 특성인 구조 열림 속도에 직접적으로 연관되어 있음을 밝혀냈다 .
또한 , 단백질이 생체 분자와 직접 결합하는 부위가 아닌 allosteric site 에서 단백질의 고유한 특성을 변화시킬 수 있음을 증명함으로써 , 생체 내 단백질들의 기능을 조절하는 새로운 방법론을 제시하였다 .
연구팀의 이번 결과는 다양한 생명현상을 관장하는 단백질의 특성을 보다 깊이 이해하는데 큰 역할을 하였으며 , 단백질의 생체분자에 대한 결합력을 결정하는 원리를 단백질의 동력학적 관점에서 입증한 것으로 평가되고 있다 .
김 학성 교수는 이번 연구에 대해 “ 지금까지는 단백질의 생체분자에 대한 결합력은 두 분자 사이의 직접적인 상호작용에 의해 결정되는 것으로 알려져 왔지만 , 본 연구를 통해 단백질의 고유한 동력학적 특성 , 즉 구조 열림 속도도 결합력을 결정하는 데 핵심적인 역할을 한다는 새로운 사실을 밝힌 것이 큰 의미가 있다 ” 라고 의의를 밝혔다 .
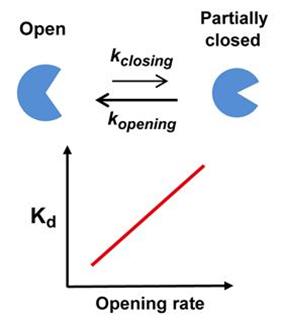
그림 1. 단백질의 안정한 상태인 열린 구조 (open) 와 불안정한 상태인 부분적으로 열린 구조 (partially closed) 사이의 전환 속도 (kopening; opening rate) 와 결합력 (Kd) 사이의 상관관계 그래프
-
연구 스스로 물체를 집고, 걷는 '실시간 프로그래밍 로봇 시트' 개발
접힘 구조는 로봇 설계에서 직관적이면서도 효율적인 형상 변형 메커니즘으로 활용되며, 우주·항공 로봇, 유연 로봇, 접이식 그리퍼(손) 등 다양한 응용이 시도되고 있다. 그러나 기존의 접힘 메커니즘은 접는 위치(hinge)나 방향이 사전에 고정돼 있어, 환경과 작업이 바뀔 때마다 구조를 새로 설계·제작해야 하는 한계가 있었다. 한국 연구진이 실시간으로 현장에 따라 프로그래밍하는‘접이식 로봇 시트 기술’을 개발해 로봇의 형태 변화 능력을 획기적으로 향상함으로써, 향후 로봇 공학 분야에 새로운 가능성을 열어줄 것으로 기대된다. 우리 대학 기계공학과 김정 교수, 박인규 교수 공동 연구팀이 형상을 실시간으로 프로그래밍할 수 있는 로봇 시트 원천 기술(field-programmable robotic folding sheet)을 개발했다고 6일 밝혔다. 이번 기술은 ‘필드 프로그래밍(field-programmability)&rs
2025-08-06 -
연구 주변 빛에너지로 24시간 건강 모니터링이 가능하다고?
심박수, 혈중산소포화도, 땀 성분 분석 등 지속적인 건강 모니터링을 위한 의료용 웨어러블 기기의 소형화와 경량화는 여전히 큰 도전 과제다. 특히 광학 센서는 LED 구동과 무선 전송에 많은 전력을 소모해 무겁고 부피가 큰 배터리를 필요로 한다. 이런 한계를 극복하기 위해 우리 연구진은 주변 빛을 에너지원으로 활용하고, 전력 상황에 따라 최적화된 관리를 통해 24시간 연속 측정이 가능한 차세대 웨어러블 플랫폼을 개발했다. 우리 대학 전기및전자공학부 권경하 교수팀이 미국 노스웨스턴대학교 박찬호 박사팀과 공동연구를 통해, 주변 빛을 활용해 배터리 전력 부담을 줄인 적응형 무선 웨어러블 플랫폼을 개발했다고 30일 밝혔다. 의료용 웨어러블 기기의 배터리 문제를 해결하기 위해, 권경하 교수 연구팀은 주변의 자연광을 에너지원으로 활용하는 혁신적인 플랫폼을 개발했다. 이 플랫폼은 세 가지 상호 보완적인 빛 에너지 기술을 통합한 것이 특징이다. 첫 번째 핵심 기술인 ‘광
2025-07-31 -
연구 빛으로 단백질 · mRNA를 원할 때 꺼내 쓴다
기존의 ‘광유전학적 분자 응축물 기술(생체 분자를 빛을 사용해 특정한 덩어리(응축체)로 뭉치게 하거나 풀리게 조절하는 기술)’은 세포 안에서 여러 단백질이나 RNA가 다양하게 섞이기 때문에 원하는 분자만 골라서 다루기 어렵다는 한계가 있었다. 이 한계를 넘어, 우리 연구진이 ‘빛’을 쪼여 세포 속 특정 단백질이나 유전정보(mRNA)를 원하는 시점에 꺼내 쓸 수 있는 기술을 개발하여 유전자 조절 기술, 신약 개발 등에서의 새로운 가능성을 제시했다. 우리 대학 생명과학과 허원도 석좌교수 연구팀이 물리학과 박용근 석좌교수 연구팀과 협력하여, 단백질 및 mRNA를 세포 내에서 빛으로 원하는 시점에 저장(Store)하고 방출(Release)할 수 있는 ‘릴리저 기술(RELISR, REversible Light-Induced Store and Release)’을 개발했다고 23일 밝혔다. 이번 연구는 세포 내 다양한 생
2025-07-23 -
연구 대기 오염 저감 위한 신개념 원자 촉매 설계
백금 셀레나이드는 백금(Pt)과 셀레늄(Se)이 층상 구조로 결합된 이차원 물질로, 우수한 결정성과 층간 상호작용의 정밀한 제어를 통해 다양한 물리적·화학적 특성의 조절이 가능한 것으로 알려져 있다. 이러한 특성으로 인해, 반도체, 광검출기, 전기화학 소자 등 다양한 분야에서 활발히 연구되어 왔다. 이번 연구진은 백금 셀레나이드 표면에 존재하는 원자 수준의 백금이 기체 반응에 대해 촉매로 기능할 수 있다는 새로운 설계 개념을 제시했으며, 이를 통해 고효율 이산화탄소 전환 및 일산화탄소 저감 등을 위한 차세대 기체상 촉매 기술로서의 가능성을 입증했다. 우리 대학 화학과 박정영 석좌교수 연구팀이 충남대학교 김현유 교수, 미국 센트럴플로리다대학교(UCF) 정연웅 교수 연구팀과 공동연구를 통해, 이차원 전이금속 칼코겐화합물인 백금 셀레나이드(PtSe₂) 표면에 노출된 백금 원자를 활용하여 우수한 일산화탄소 산화 성능을 구현하는 데 성공했다고 22일 밝혔다. 연구진은
2025-07-22 -
연구 음주로 인한 간염 유발 원리 최초 밝혔다
과도한 음주는 알코올성 간질환을 유발하며, 이 중 약 20%는 알코올 지방간염으로 진행되고 이는 간경변증과 간부전으로 이어질 수 있어 조기 진단과 치료가 매우 중요하다. 우리 연구진은 음주 시 활성산소(ROS)가 발생해 간세포 사멸과 염증 반응을 유발하는 새로운 분자 메커니즘을 규명했다. 아울러, 간세포가 신경계의 시냅스처럼 신호를 주고 받는 유사시냅스를 형성하고 염증을 유도하는 ‘새로운 신경학적 경로’를 세계 최초로 밝혀냈다. 우리 대학 의과학대학원 정원일 교수 연구팀이 서울대 보라매 병원 김원 교수 연구팀과의 공동 연구를 통해, 음주로 인한 간 손상 및 염증(알코올 지방간염, Alcohol-associated Steatohepatitis, ASH)의 발생 기전을 분자 수준에서 규명해 알코올 간질환의 진단과 치료에 단서를 제시했다고 17일 밝혔다. 정원일 교수 연구팀은 만성 음주 시 ‘소포성 글루탐산 수송체(VGLUT3)’의 발
2025-07-17