%EC%B2%AD%EC%83%89%EA%B4%91
-
 입을 수 있는 OLED로 소아 황달 치료기술 개발
우리 대학 전기및전자공학부 최경철 교수 연구팀이 을지대학교 병원(김승연 교수, 임춘화 교수), 가천대학교(전용민 교수), 선문대학교(권정현 교수)와의 공동 연구를 통해 실제 직물 기반의 웨어러블 청색 OLED를 개발하고, 황달 질환을 앓는 신생아의 혈청에서 청색 OLED 광원에 의한 *빌리루빈 감소로 인한 황달 치료 효과를 확인했다고 22일 밝혔다.
☞ 빌리루빈: 혈액에서 산소를 공급해주는 적혈구가 수명을 다해 분해된 결과물로, 보통 간에 의해 해독되고 담즙으로 배설된다. 혈장 내 빌리루빈의 농도가 올라가면 피부와 눈의 흰자위가 누런색을 띠는 황달 증상이 나타난다. 신생아는 수명이 짧은 적혈구를 갖고 있으나 간 대사가 미숙해 빌리루빈을 많이 생산한다.
최경철 교수 연구실의 최승엽 박사, 가천대학교 의공학과 전용민 교수, 선문대학교 권정현 교수가 공동 제1 저자로 참여한 이번 연구는 첨단 과학기술 분야의 국제 저명 학술지인 `어드밴스드 사이언스(Advanced Science)'에 지난 10월 30일 게재되었고, 속 표지 논문으로 선정됐다.
신생아의 황달 치료는 광선 요법, 약물 투여, 교환 수혈 등 다양한 방법으로 시행된다. 이 중 광선 요법은 체내에 축적된 빌리루빈을 빛에 노출해 변형시켜 체외로 방출하는 안전하고 효과적인 치료 방법이다. 대부분의 신생아 황달은 광선 요법으로 치료할 수 있어 가장 널리 활용되고 있다.
병원에서는 신생아의 혈액 내 빌리루빈 농도가 치료 범위를 초과하면 신생아를 신생아 집중치료실(NICU)에 입원시켜 인큐베이터의 스탠드에 장착된 청색 LED의 빛으로 치료한다. 이 방법은 신생아 황달 증상을 완화하는 데 매우 효과적이지만 신생아를 부모로부터 격리하고 치료하는 동안 모유 수유 중단, 청색광에 의한 망막 손상 방지를 위해 신생아의 눈은 반드시 눈가리개로 완전히 가려야 하는 등의 문제와 더불어 기존에는 LED 기반 설치형 플랫폼이 사용돼 웨어러블 치료 적용에 한계가 있었다.
최경철 교수 연구팀은 황달 치료에 효과적인 470nm(나노미터) 파장의 고출력 고신뢰성의 청색 OLED를 사람이 착용 가능한 직물 위에 구현했으며, 직물과 같은 높은 유연성을 유지하는 옷 OLED 소아 황달 치료 플랫폼을 개발했다. 직물 기반의 청색 OLED는 4V 미만의 저전압에서도 황달치료에 충분한 출력(> 20 μW/cm2/nm)을 확보했을 뿐만 아니라 100시간 이상의 구동 수명, 35℃ 미만의 낮은 구동 온도, 물세탁 신뢰성, 2mm(밀리미터) 수준의 낮은 곡률 반경에서 1,000회 이상을 견디는 유연성 등의 신뢰성을 확보할 수 있었다.
이번 연구에서 470nm 파장을 갖는 청색 OLED를 신생아의 혈청에 조사했을 시, 3시간 이내에 황달 치료가 완료됐다고 판단되는 빌리루빈 수치(12 mg/dL)에 도달했으며, 기존 병원에서 활용되는 LED 황달 상용 치료기기 대비 균일하면서도 효과적인 황달 치료 성능을 연구팀은 확인했다.
공동 제1 저자인 최승엽 박사, 전용민 교수(가천대), 권정현 교수(선문대)는 "이번 연구를 통해 실제 신생아가 착용해 황달 치료가 가능한 성능 및 신뢰성을 갖는 섬유 기반의 청색 OLED 개발에 성공했다ˮ며 "설치형 LED 치료기기의 단점을 보완하며 더욱 균일한 효과를 기대할 수 있는 웨어러블 황달 치료 기술이 상용화될 수 있는 기반을 마련했다ˮ고 말했다.
최경철 교수는 "OLED 분야는 우리나라가 최고 기술을 보유하고 있지만, 중국의 기술 추격이 예사롭지 않은 이 시점에, OLED의 다양한 응용 기술을 개발하는 것이 중국과의 OLED 기술격차를 더 벌릴 수 있고, OLED 응용 중, 직물 위 OLED 기반 웨어러블 의료 기술개발로 바이오 헬스케어 시대에 맞는 OLED 응용의 새로운 시장을 개척해, 우리나라의 OLED 기술이 계속 선두를 유지하기를 바란다ˮ라고 말했다.
이번 연구는 과학기술정보통신부 한국연구재단의 선도연구센터 사업의 지원으로 수행됐다.
2022.11.22 조회수 4281
입을 수 있는 OLED로 소아 황달 치료기술 개발
우리 대학 전기및전자공학부 최경철 교수 연구팀이 을지대학교 병원(김승연 교수, 임춘화 교수), 가천대학교(전용민 교수), 선문대학교(권정현 교수)와의 공동 연구를 통해 실제 직물 기반의 웨어러블 청색 OLED를 개발하고, 황달 질환을 앓는 신생아의 혈청에서 청색 OLED 광원에 의한 *빌리루빈 감소로 인한 황달 치료 효과를 확인했다고 22일 밝혔다.
☞ 빌리루빈: 혈액에서 산소를 공급해주는 적혈구가 수명을 다해 분해된 결과물로, 보통 간에 의해 해독되고 담즙으로 배설된다. 혈장 내 빌리루빈의 농도가 올라가면 피부와 눈의 흰자위가 누런색을 띠는 황달 증상이 나타난다. 신생아는 수명이 짧은 적혈구를 갖고 있으나 간 대사가 미숙해 빌리루빈을 많이 생산한다.
최경철 교수 연구실의 최승엽 박사, 가천대학교 의공학과 전용민 교수, 선문대학교 권정현 교수가 공동 제1 저자로 참여한 이번 연구는 첨단 과학기술 분야의 국제 저명 학술지인 `어드밴스드 사이언스(Advanced Science)'에 지난 10월 30일 게재되었고, 속 표지 논문으로 선정됐다.
신생아의 황달 치료는 광선 요법, 약물 투여, 교환 수혈 등 다양한 방법으로 시행된다. 이 중 광선 요법은 체내에 축적된 빌리루빈을 빛에 노출해 변형시켜 체외로 방출하는 안전하고 효과적인 치료 방법이다. 대부분의 신생아 황달은 광선 요법으로 치료할 수 있어 가장 널리 활용되고 있다.
병원에서는 신생아의 혈액 내 빌리루빈 농도가 치료 범위를 초과하면 신생아를 신생아 집중치료실(NICU)에 입원시켜 인큐베이터의 스탠드에 장착된 청색 LED의 빛으로 치료한다. 이 방법은 신생아 황달 증상을 완화하는 데 매우 효과적이지만 신생아를 부모로부터 격리하고 치료하는 동안 모유 수유 중단, 청색광에 의한 망막 손상 방지를 위해 신생아의 눈은 반드시 눈가리개로 완전히 가려야 하는 등의 문제와 더불어 기존에는 LED 기반 설치형 플랫폼이 사용돼 웨어러블 치료 적용에 한계가 있었다.
최경철 교수 연구팀은 황달 치료에 효과적인 470nm(나노미터) 파장의 고출력 고신뢰성의 청색 OLED를 사람이 착용 가능한 직물 위에 구현했으며, 직물과 같은 높은 유연성을 유지하는 옷 OLED 소아 황달 치료 플랫폼을 개발했다. 직물 기반의 청색 OLED는 4V 미만의 저전압에서도 황달치료에 충분한 출력(> 20 μW/cm2/nm)을 확보했을 뿐만 아니라 100시간 이상의 구동 수명, 35℃ 미만의 낮은 구동 온도, 물세탁 신뢰성, 2mm(밀리미터) 수준의 낮은 곡률 반경에서 1,000회 이상을 견디는 유연성 등의 신뢰성을 확보할 수 있었다.
이번 연구에서 470nm 파장을 갖는 청색 OLED를 신생아의 혈청에 조사했을 시, 3시간 이내에 황달 치료가 완료됐다고 판단되는 빌리루빈 수치(12 mg/dL)에 도달했으며, 기존 병원에서 활용되는 LED 황달 상용 치료기기 대비 균일하면서도 효과적인 황달 치료 성능을 연구팀은 확인했다.
공동 제1 저자인 최승엽 박사, 전용민 교수(가천대), 권정현 교수(선문대)는 "이번 연구를 통해 실제 신생아가 착용해 황달 치료가 가능한 성능 및 신뢰성을 갖는 섬유 기반의 청색 OLED 개발에 성공했다ˮ며 "설치형 LED 치료기기의 단점을 보완하며 더욱 균일한 효과를 기대할 수 있는 웨어러블 황달 치료 기술이 상용화될 수 있는 기반을 마련했다ˮ고 말했다.
최경철 교수는 "OLED 분야는 우리나라가 최고 기술을 보유하고 있지만, 중국의 기술 추격이 예사롭지 않은 이 시점에, OLED의 다양한 응용 기술을 개발하는 것이 중국과의 OLED 기술격차를 더 벌릴 수 있고, OLED 응용 중, 직물 위 OLED 기반 웨어러블 의료 기술개발로 바이오 헬스케어 시대에 맞는 OLED 응용의 새로운 시장을 개척해, 우리나라의 OLED 기술이 계속 선두를 유지하기를 바란다ˮ라고 말했다.
이번 연구는 과학기술정보통신부 한국연구재단의 선도연구센터 사업의 지원으로 수행됐다.
2022.11.22 조회수 4281 -
 허원도 교수, 빛으로 단백질군집형성 속도 10배 높이는 새 광유전학 기술 개발
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀이 청색광 수용 단백질인 크립토크롬2(Cryptochrome2)를 변형한 크립토크롬2 클러스트(CRY2clust)를 개발했다.
이를 통해 기존에 비해 약 10배 더 빠른 반응속도로 단백질 군집을 형성하는 데 성공했다.
이번 연구결과는 네이처 자매지인 ‘네이처 커뮤니케이션즈(Nature Communications)’ 23일자에 게재됐다.
세포막 단백질이나 신호전달 단백질, 효소 등 많은 단백질은 자신들끼리 서로 군집을 이룰 때 제 기능이 활성화된다. 그 동안 화학물질을 이용해 단백질 군집 형성을 유도하려는 노력이 이뤄져왔으나 부작용과 시간적 제약 등 한계가 있었다.
광유전학 분야 연구자들은 화학물질을 사용하지 않는 대신 빛을 이용해 단백질 군집을 형성하고자 식물의 청색광 수용 단백질인 크립토크롬2를 활용했다.
허원도 교수 연구팀은 크립토크롬2의 일부 구조를 변형해 기존 크립토크롬2를 활용한 광유전학 기술보다 단백질 군집을 더 빠르게 만들 수 있는 방법을 찾았다.
크립토크롬2의 단백질 사슬 C말단(C-terminal)에 9개의 아미노산 잔기로 구성된 매우 짧은 펩티드(Peptide)를 부착하자 일반 크립토크롬2보다 빛에 10배 이상 더 빠르게 반응한다는 사실을 관찰한 것이다.
연구진은 이 기술을 CRY2clust라 이름 붙였다.
연구팀은 과거 자체 개발한 광유전학 기술에 CRY2clust를 접목해 CRY2을 이용한 기존 시스템과의 단백질 활성 효율의 차이를 확인했다. CRY2clust를 사용하면 빛으로 세포막의 칼슘이온채널을 훨씬 빠르게 끄고 켜거나(광유도 칼슘이온채널 활성 시스템 ; OptoSTIM1) 신경세포의 분화를 더욱 효율적으로 조절(광유도 신경성장인자 수용체 활성 시스템 ; OptoTrkB)할 수 있었다.
연구진은 더 나아가 실험실에서 단백질 군집 형성에 주로 활용하는 여러 형광단백질(Fluorescent protein)과 크립토크롬2를 짝지어 결합해봄으로써 빛을 이용해 단백질 군집을 더 효율적으로 만들 수 있는 조합의 조건을 찾았다.
형광단백질이 하나보다는 여러 개가 결합한 형태일수록 빛을 비추었을 때 광유도 클러스트를 더욱 높은 비율로 형성했다. 또한 형광단백질을 크립토크롬2의 단백질 사슬 말단 중 N말단이 아닌 C말단에 붙이는 경우 광유도 클러스트 형성 효율이 더 높은 것으로 확인됐다. 단백질 군집이 잘 형성되는 조건을 찾았다는 점에서 연구자의 실험 선택의 폭을 넓혀준 데 의의가 있다.
허원도 교수 연구팀은 CRY2clust를 개발해 빛을 이용한 단백질의 활성을 훨씬 효율적으로 유도하는데 성공했다.
허원도 교수는 “이번 연구에서 개발한 CRY2clust는 향후 광유전학 분야의 실험에 유용한 도구가 될 것이다”며“다양한 형광단백질-CRY2 조합을 통해 찾은 단백질 군집 형성 성공 요인은 광유전학 시스템 개발에 길잡이 역할을 할 것이다”고 말했다.
□ 그림 설명
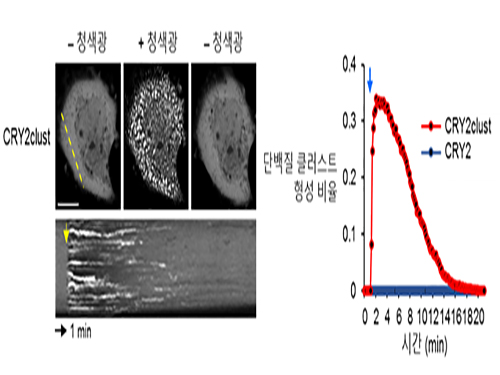
그림1. 기존 크립토크롬2 대비 CRY2clust의 단백질 군집 형성 속도
그림2. CRY2clust 시스템을 적용한 광유도 단백질 기능 조절
그림3. 형광단백질을 이용한 다양한 단백질 군집 형성
2017.06.26 조회수 10571
허원도 교수, 빛으로 단백질군집형성 속도 10배 높이는 새 광유전학 기술 개발
〈 허 원 도 교수 〉
우리 대학 생명과학과 허원도 교수 연구팀이 청색광 수용 단백질인 크립토크롬2(Cryptochrome2)를 변형한 크립토크롬2 클러스트(CRY2clust)를 개발했다.
이를 통해 기존에 비해 약 10배 더 빠른 반응속도로 단백질 군집을 형성하는 데 성공했다.
이번 연구결과는 네이처 자매지인 ‘네이처 커뮤니케이션즈(Nature Communications)’ 23일자에 게재됐다.
세포막 단백질이나 신호전달 단백질, 효소 등 많은 단백질은 자신들끼리 서로 군집을 이룰 때 제 기능이 활성화된다. 그 동안 화학물질을 이용해 단백질 군집 형성을 유도하려는 노력이 이뤄져왔으나 부작용과 시간적 제약 등 한계가 있었다.
광유전학 분야 연구자들은 화학물질을 사용하지 않는 대신 빛을 이용해 단백질 군집을 형성하고자 식물의 청색광 수용 단백질인 크립토크롬2를 활용했다.
허원도 교수 연구팀은 크립토크롬2의 일부 구조를 변형해 기존 크립토크롬2를 활용한 광유전학 기술보다 단백질 군집을 더 빠르게 만들 수 있는 방법을 찾았다.
크립토크롬2의 단백질 사슬 C말단(C-terminal)에 9개의 아미노산 잔기로 구성된 매우 짧은 펩티드(Peptide)를 부착하자 일반 크립토크롬2보다 빛에 10배 이상 더 빠르게 반응한다는 사실을 관찰한 것이다.
연구진은 이 기술을 CRY2clust라 이름 붙였다.
연구팀은 과거 자체 개발한 광유전학 기술에 CRY2clust를 접목해 CRY2을 이용한 기존 시스템과의 단백질 활성 효율의 차이를 확인했다. CRY2clust를 사용하면 빛으로 세포막의 칼슘이온채널을 훨씬 빠르게 끄고 켜거나(광유도 칼슘이온채널 활성 시스템 ; OptoSTIM1) 신경세포의 분화를 더욱 효율적으로 조절(광유도 신경성장인자 수용체 활성 시스템 ; OptoTrkB)할 수 있었다.
연구진은 더 나아가 실험실에서 단백질 군집 형성에 주로 활용하는 여러 형광단백질(Fluorescent protein)과 크립토크롬2를 짝지어 결합해봄으로써 빛을 이용해 단백질 군집을 더 효율적으로 만들 수 있는 조합의 조건을 찾았다.
형광단백질이 하나보다는 여러 개가 결합한 형태일수록 빛을 비추었을 때 광유도 클러스트를 더욱 높은 비율로 형성했다. 또한 형광단백질을 크립토크롬2의 단백질 사슬 말단 중 N말단이 아닌 C말단에 붙이는 경우 광유도 클러스트 형성 효율이 더 높은 것으로 확인됐다. 단백질 군집이 잘 형성되는 조건을 찾았다는 점에서 연구자의 실험 선택의 폭을 넓혀준 데 의의가 있다.
허원도 교수 연구팀은 CRY2clust를 개발해 빛을 이용한 단백질의 활성을 훨씬 효율적으로 유도하는데 성공했다.
허원도 교수는 “이번 연구에서 개발한 CRY2clust는 향후 광유전학 분야의 실험에 유용한 도구가 될 것이다”며“다양한 형광단백질-CRY2 조합을 통해 찾은 단백질 군집 형성 성공 요인은 광유전학 시스템 개발에 길잡이 역할을 할 것이다”고 말했다.
□ 그림 설명
그림1. 기존 크립토크롬2 대비 CRY2clust의 단백질 군집 형성 속도
그림2. CRY2clust 시스템을 적용한 광유도 단백질 기능 조절
그림3. 형광단백질을 이용한 다양한 단백질 군집 형성
2017.06.26 조회수 10571